Xx Güzeldi 2022-05-31
Kimyasal Bağlar (İyonik ve Kovalent Bağ)
Atom ve molekülleri bir arada tutan kuvvete kimyasal bağ denir.Kimyasal bağlar kovalent bağ ve iyonik bağ olmak üzere iki ana grupta toplanır.
İyonik Bağ
Bir metâl ile bir ametâl arasında elektron alışverişiyle oluşan bağa iyonik bağ denir.
Elektron veren element verdiği elektron sayısı kadar (+) iyon, elektron alan element aldığı elektron sayısı kadar (–) iyon değerliği kazanır.
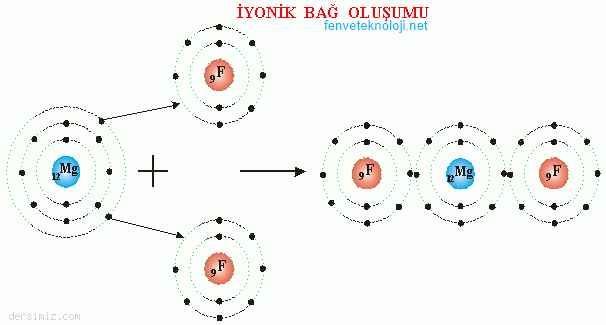
Örnek: Magnezyum atomunun son yörüngesinde iki, Flor atomunun son yörüngesinde yedi elektron vardır.
Magnezyum Florür bileşiği oluşurken, magnezyum atomu son yörüngesindeki iki elektronunu verir. Oktet kuralına uyarak son yörüngesindeki elektron sayısını sekize tamamlar. Bu iki elektronun her birini bir flor atomu alır. Flor atomları da oktet kuralına uyarak son yörüngelerindeki elektron sayılarını sekize tamamlarlar.
Elektron alışverişinden sonra magnezyum atomu (+2) iyon, flor atomları (– 1) iyon haline geçerler.. Zıt elektrikle yüklenen magnezyum ve flor atomları birbirlerini çekerler. Böylece aralarında iyonik bağ oluşur.
Kovalent Bağ
İki ametal arasında elektronların ortaklaşa kullanımıyla oluşan bağa kovalent bağ denir.Polar ve apolar kovalent bağ olmak üzere iki çeşittir.
POLAR KOVALENT BAĞ :
Farkı cins iki ametâl atomu arasında elektronların ortaklaşa kullanımıyla oluşan bağa polar kovalent bağ denir.
Polar kovalent bağ oluşumunda atomlar arasında elektron alış– verişi olmaz. Son yörüngelerdeki elektronlar ortaklaşa kullanılır. Polar kovalent bağ sonucunda oluşan molekül bileşik molekülüdür.
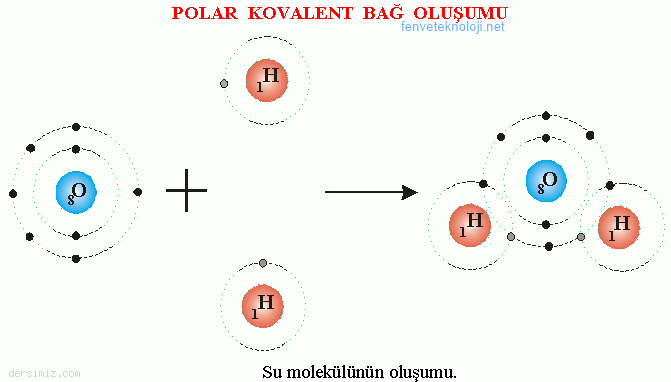
Örnek : Oksijen atomunun son enerji seviyesinde altı elektron, hidrojen atomunun tek olan enerji seviyesinde bir elektron vardır.
Su molekülü oluşurken, iki hidrojen atomu ve bir oksijen atomunun son yörüngeleri şekildekine benzer girişim yapar. Oksijen atomu son yörüngesindeki elektron sayısını sekize, hidrojen atomları ikiye tamamlar.Böylece hidrojen ve oksijen atomları son yörüngelerdeki elektronları ortaklaşa kullanarak aralarında polar kovalent bağ oluştururlar
APOLAR KOVALENT BAĞ :
Aynı cins iki ametâl atomu arasında elektronların ortaklaşa kullanımıyla oluşan bağa apolar kovalent bağ denir.
Apolar kovalent bağ ile oluşan molekül element molekülüdür. Soy gazlar hariç, diğer gaz halindeki elementlerin molekülleri arasındaki bağ apolar kovalent bağdır.
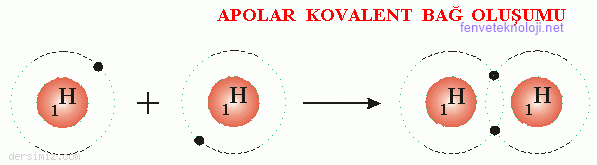
Örnek : Hidrojen gazının oluşumunda iki hidrojen atomunun yörüngeleri şekildekine benzer girişim yaparak elektronlarını ortaklaşa kullanırlar. Böylece iki hidrojen atomu apolar kovalent bağ ile bağlanarak yörüngelerindeki elektron sayılarını ikiye tamamlarlar.
![]() dersimiz.com
dersimiz.com
![]() İyonik Bağ oluşumu kovalent bağ oluşumu Kimyasal Bağlar polar kovalent bağ apolar kovalent bağ örnekler fen ve teknoloji ders notu konu özeti çalışma notları özetler ders anlatım eğitim öğretim kaynakları
İyonik Bağ oluşumu kovalent bağ oluşumu Kimyasal Bağlar polar kovalent bağ apolar kovalent bağ örnekler fen ve teknoloji ders notu konu özeti çalışma notları özetler ders anlatım eğitim öğretim kaynakları
Benzer Fen Bilimleri Ders Notları
- Gregor Mendel ve Kalıtımla İlgili Temel Kavramlar
- Vitaminler ve Bu Vitaminlerin Görevleri Nelerdir?
- Besin Zinciri
- Mikroskobik Canlılar
- Sindirim Sistemi Organları ve Görevleri
- Basit Makineler ve Makaralar
- + Ders Notları Ekleyin
- Ders Notları Ana Sayfa
Kimyasal Bağlar (İyonik ve Kovalent Bağ) Hakkında Yorum Yazın...
Kimyasal Bağlar (İyonik ve Kovalent Bağ) Hakkında Yazılan Yorumlar
İçerikle ilgili 111 yorum yazılmış.